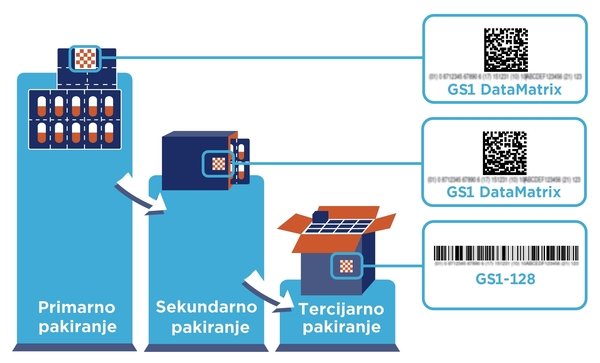
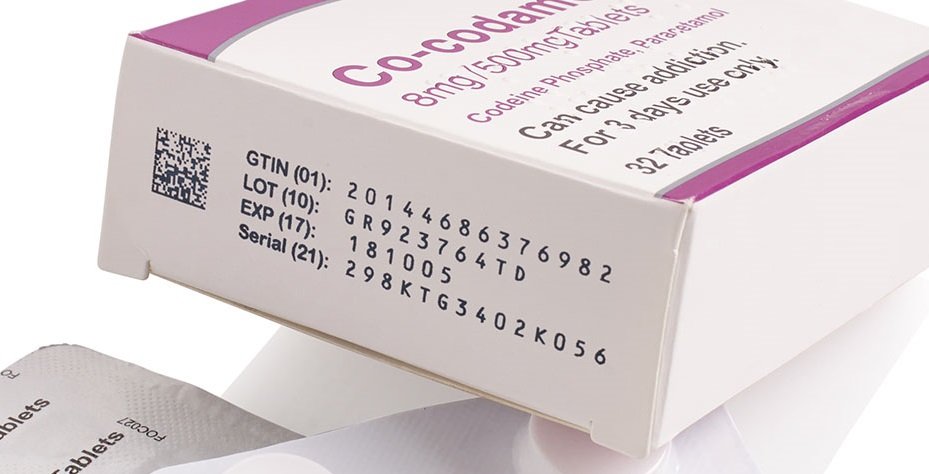
U farmaceutskom sektoru sljedivost znači praćenje svakog lijeka od njegove proizvodnje do pacijenta, a to se najučinkovitije postiže korištenjem globalnih standarda i dvodimenzionalnih barkodova. Direktivom 2011/62/EU (FMD) i Delegiranom uredbom EU 2016/161 zahtijevaju se sigurnosna svojstva i jedinstvena identifikacija lijekova koji se izdaju na recept na razini cijele Europske unije. Cilj je učiniti europsko tržište lijekovima sigurnijim, tj. spriječiti ulazak krivotvorenih lijekova u legalan opskrbni lanac. Rok za provedbu u zemljama članicama EU-a bio je 9. veljače 2019.
Barkod
Barkod
GS1 standardi
GS1 standardi
Proizvodi
Jedinični proizvod i transportna kutija
Varijabilna mjera (CRO-SCAN)
Proizvodi s promjenjivom mjerom (vagani)
Palete
SSCC, GS1-128 i logistička naljepnica
Lokacije
GLN - Globalni lokacijski broj
Online trgovine
Prodaja na online platformama kao što su Amazon, eBay, AliExpress, Google Shopping
Servisi
Servisi